利用碱式碳酸铜制备氧化铜及产物的实验检验
在化学实验室中,我们可利用碱式碳酸铜(化学式为Cu₂(OH)₂CO₃)为原料,通过加热分解来制备氧化铜(CuO),并进一步利用碳粉进行还原实验。这是一个经典的、能串联多个化学反应与物质检验的综合实验。
实验一:制备氧化铜并检验产物
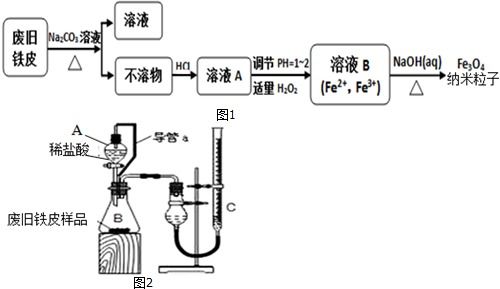
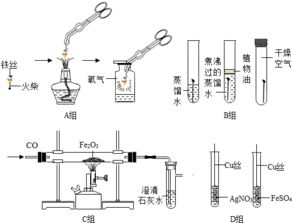
实验装置:如图所示,实验装置通常包括热源(如酒精灯)、硬质玻璃管(内装碱式碳酸铜)、导管以及用于检验产物的部分(如澄清石灰水)。装置中标注了a和b两个连接点。
实验步骤与原理:
1. 连接与通气:按照图示连接好装置各部件,确保气密性良好。连接a和b,并打开活塞,通入空气。此步骤的目的在于排尽装置内的空气(特别是二氧化碳),防止对后续产物检验造成干扰,同时提供稳定的气流环境。
2. 加热分解:点燃酒精灯,对盛有碱式碳酸铜的硬质玻璃管进行加热。碱式碳酸铜受热分解,发生如下反应:
Cu₂(OH)₂CO₃ → 2CuO + H₂O↑ + CO₂↑
绿色粉末状的碱式碳酸铜逐渐转变为黑色的氧化铜固体,同时生成水蒸气和二氧化碳气体。
- 产物检验:
- 固体产物检验:待玻璃管冷却后,可取出黑色固体,加入稀硫酸。若黑色固体溶解形成蓝色溶液(生成硫酸铜溶液),则可证明固体产物为氧化铜。
- 气体产物检验:分解产生的混合气体通过导管导出。
- 水蒸气:通常在装置中可通过观察干燥玻璃管或U形管前端出现水珠,或使用无水硫酸铜变蓝来检验。
- 二氧化碳:气体通入澄清石灰水中,若观察到石灰水变浑浊,则证明有二氧化碳生成。
步骤一(通入空气)的深入分析:在加热前通入空气(或更常用的惰性气体如氮气),核心目的是“驱赶”或“置换”装置中原有的空气。这样做有几个关键作用:
排除干扰:装置内空气中的二氧化碳会与澄清石灰水反应,导致在加热前就出现浑浊,干扰对反应生成二氧化碳的准确检验。先通入气体将其排出,可确保后续观察到的浑浊现象 solely(完全)来自于碱式碳酸铜的分解。
安全与纯净:防止空气中的氧气在加热条件下与可能产生的其他物质(或后续碳粉还原实验中的碳粉)发生副反应,确保反应在预期的氛围下进行,使产物更纯净。
* 引导气流:建立起从进气端到出气端的稳定气流,确保生成的气体能被顺利、完全地导向后续的检验装置,提高检验的灵敏度和准确性。
实验拓展:碳粉还原氧化铜
在成功制得氧化铜后,可利用其进行碳粉还原实验。将上述得到的黑色氧化铜粉末与碳粉(通常为木炭粉)按一定比例混合,放入硬质玻璃管中再次加强热。发生的主要反应为:2CuO + C → 2Cu + CO₂↑
现象与检验:
1. 黑色混合物中逐渐出现紫红色有金属光泽的物质(铜单质)。
2. 将生成的气体通入澄清石灰水,石灰水变浑浊,证明有二氧化碳生成。
###
本实验从碱式碳酸铜出发,通过加热分解制备氧化铜,并系统地检验了固态和气态产物。实验前的通气处理是保证实验现象准确、结论可靠的关键步骤。制备出的氧化铜又可作为原料进行碳的还原性实验,体现了化学实验中物质的转化与性质的递进探究。整个过程融合了物质制备、性质验证和实验设计思维,是一个极具教学价值的综合实验。
如若转载,请注明出处:http://www.jifangkeji.com/product/11.html
更新时间:2026-05-01 09:25:33