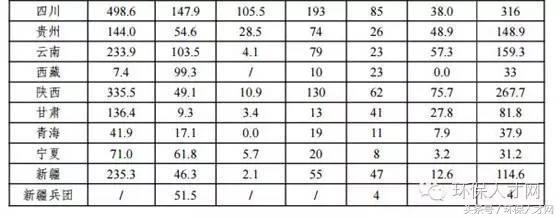
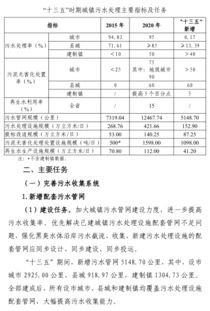
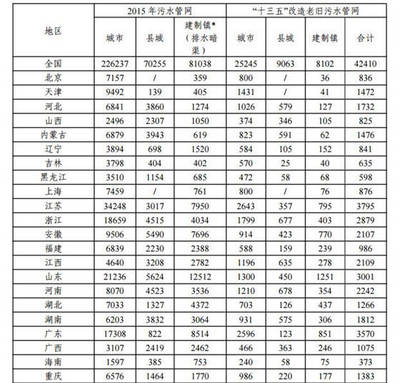
验证MnO₂在KClO₃受热分解制O₂反应前后质量不变的实验设计与分析
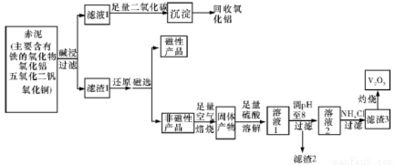
为了验证MnO₂在KClO₃受热分解制取O₂的反应前后质量是否改变,某兴趣小组设计了如下实验,并探讨了相关操作和工业应用。
1. 实验装置与气密性检查
实验装置通常包括铁架台、酒精灯、试管(或硬质玻璃管)、导管、水槽和集气瓶等。其中,MnO₂和KClO₃的混合物置于试管中加热,生成的氧气通过导管收集。
检查装置气密性的方法:
首先将导管末端浸入水槽的水中,然后用手紧握试管(或用酒精灯微热),使试管内空气受热膨胀。如果观察到导管口有气泡冒出,松开手(或停止加热)后,导管内形成一段稳定的水柱,则说明装置气密性良好。这是利用热胀冷缩原理的常规检查方法。
2. 实验步骤与数据分析
实验操作:
取2.45 g KClO₃固体粉末与适量MnO₂(作为催化剂)混合均匀,装入试管中加热。反应结束后,待试管冷却,分离出剩余的MnO₂,干燥后称量其质量。理论上,MnO₂在反应中不参与化学变化,仅加快反应速率,因此反应前后其质量应保持不变。
数据验证:
已知KClO₃的相对分子质量为122.5,2.45 g恰好为0.02 mol。在MnO₂催化下,KClO₃受热分解的化学方程式为:
2KClO₃ → 2KCl + 3O₂↑
根据化学计量,0.02 mol KClO₃完全分解可生成0.03 mol O₂,即约0.96 g氧气。实验中,通过收集氧气的体积或质量变化,可间接验证反应是否完全,进而说明MnO₂的催化作用。称量反应前后MnO₂的质量,若基本一致(允许微小误差),则证明其质量不变。
3. 污水处理及其再生利用的联系
此实验虽为化学基础验证,但涉及的物质与环保技术相关。例如:
- MnO₂的应用:二氧化锰不仅作为催化剂,在污水处理中也可用作氧化剂或吸附剂,帮助去除有机污染物和重金属离子。
- 氧气的意义:制取的氧气在污水处理中用于曝气过程,促进微生物分解有机物,提升水质。
- 资源再生:通过实验验证催化剂的可重复使用性,体现了绿色化学理念,这与污水再生利用中“减少废弃物、循环利用”的原则相通。
4. 结论
通过规范操作,如检查装置气密性以确保实验准确性,并对比反应前后MnO₂的质量,可有效验证其在KClO₃分解反应中的催化作用和质量守恒。这一原理在环境保护和资源再生领域具有借鉴价值,强调了化学实验与实际应用的结合。
如若转载,请注明出处:http://www.jifangkeji.com/product/24.html
更新时间:2026-05-15 03:00:12